全内半月板缝合系统通常由植入物和配套工具组成。植入物包括固定锚(棒)和缝线,配套工具包括插入器等。固定锚(棒)通常采用聚醚醚酮材料制成,缝线通常采用超高分子量聚乙烯(或为主)材料制成,插入器通常由手柄和不锈钢材料的针杆制成。在我国归属于第三类医疗器械注册管理,本文为大家介绍全内半月板缝合系统产品技术要求及注册注意事项。
全内半月板缝合系统通常由植入物和配套工具组成。植入物包括固定锚(棒)和缝线,配套工具包括插入器等。固定锚(棒)通常采用聚醚醚酮材料制成,缝线通常采用超高分子量聚乙烯(或为主)材料制成,插入器通常由手柄和不锈钢材料的针杆制成。在我国归属于第三类医疗器械注册管理,本文为大家介绍全内半月板缝合系统产品技术要求及注册注意事项。
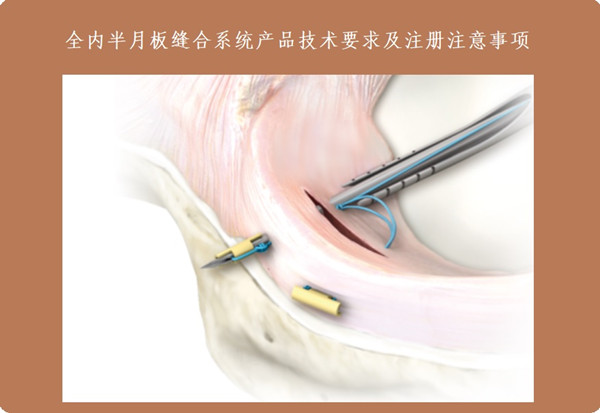
一、全内半月板缝合系统产品技术要求
全内半月板缝合系统产品技术要求需参考《医疗器械产品技术要求编写指导原则》的相关要求编制。产品技术要求需符合相关标准及法律法规的要求,同时也要结合产品的设计属性制定保证产品安全、有效的产品技术要求,全内半月板缝合系统技术要求中的性能指标可以参考以下列举的项目进行制定,并结合申报产品特点选择或增加适用的性能指标:
1.固定锚(棒):外观、表面粗糙度、表面缺陷、尺寸、硬度(如适用);
2.缝线:外观、线径、长度、断裂强力、褪色试验;
3.插入器:刺穿力、外观、表面粗糙度、硬度、耐腐蚀性能;
4.系统固定强度、无菌、环氧乙烷残留量。
此外,金属材料的化学成分和显微组织、聚合物材料的理化性能、阳极氧化表面元素定性分析等适用内容应在产品技术要求附录中予以规定,并提供相应的支持性资料。该部分内容需要注意的是,技术要求中性能指标的制定要全面,同时需根据产品临床需求和生产质控水平制定性能指标的可接受限值,比如在既往的审评过程中,申请人在制定缝线的断裂强力指标接受限值时,往往直接采用YY 0167-2020《非吸收性外科缝线》中的接受限值,但全内半月板缝合系统中的缝线与外科缝线的预期用途存在较大差异,其设计预期并非单纯用于人体组织缝合,而需承担固定半月板的拉力,与外科缝线在缝线强度上要求不同,因此,审评过程中会要求申请人结合产品临床需求和生产质控水平重新制定缝线断裂强力的接受限值。
二、全内半月板缝合系统产品注册注意事项
对于拟上市的全内半月板缝合系统,需提供产品的非临床研究资料,包括功能性、安全性指标以及与质量控制相关的其他指标的确定依据。全内半月板缝合系统的非临床研究需着重从性能研究、生物相容性、动物试验、灭菌确认和稳定性等方面考虑。非临床研究部分也是注册申报的难点,申报资料存在问题较多,申请人需重点关注。
1.性能研究
全内半月板缝合系统的结构设计若不合理将导致产品在临床使用中出现功能失效(如产品发生永久变形导致失效或不能充分承受载荷),无法完成其临床预期功能。开展充分的性能研究,是评估产品功能失效风险的重要手段,也是产品设计验证的重要环节。在全内半月板缝合系统的研发阶段,需根据产品特点及同类产品临床上的不良事件确定相关失效风险源。目前很多国家已建立了医疗器械不良事件监测系统,美国的MAUDE数据库属于全数据库,收录了按照FDA法规进行报告的所有不良事件,信息量较大。通过检索MAUDE数据库,以在境内外同时上市、国产化程度较高的部分半月板缝合系统为目标,汇总了从2016年到2021年的不良事件共520条。根据全内半月板缝合系统不良事件汇总结果,此类产品功能失效的风险点主要集中在固定锚(棒)无法击发或提前击发、插入器断裂或变形、缝线断裂、固定锚(棒)断裂、固定失效等方面,与产品的操作使用性能、插入器强度、缝线强度、系统固定强度直接相关,上述性能也是注册技术审评重点关注的一些指标,下面给出上述性能指标的一些思考。
(1)全内半月板缝合系统的操作使用性能:根据不良事件汇总结果,全内半月板缝合系统的主要失效模式是无法正常击发(包括无法击发或提前击发),表明全内半月板缝合术的成功与否很大程度取决于配套手术器械与植入物作为整体的操作使用性能,手术器械对于手术成功与否及手术时间长短有很大影响,手术器械是否操作简便并能正确发挥其预期性能十分关键。针对全内半月板缝合系统进行操作使用测试是完成产品设计确认的工作之一。操作使用性能研究的观察指标通常包括植入物挡板在手术器械中的部署是否合理及能否顺利击发、插入器能否顺利刺穿半月板并不发生断裂或变形、深度限定器能否准确限位、手术器械能否顺利回退、推结器能否顺利完成打结等。在开展操作使用性能研究时可选取离体生物半月板(如猪半月板等)进行模拟临床手术操作,需注意样本量计算、操作人员培训、评价指标设定等内容。
(2)插入器强度:根据不良事件汇总结果,如果插入器断裂或发生较大程度的变形将无法正常击发固定锚(棒)并导致手术的失败,插入器强度是否足够直接决定了缝合系统能否顺利穿透半月板并顺利击发。插入器强度可通过刚性、韧性、刺穿力指标进行量化。目前国内外尚未建立全内半月板缝合系统相关标准,在开展该部分研究时可参考具有类似功能的手术器械标准中的方法,如YY/T 0043-2016《医用缝合针》、YY/T 1148-2009《腰椎穿刺针》等。
(3)缝线强度:根据不良事件汇总结果,全内半月板缝合系统在收紧两个固定锚(棒)时会有缝线断裂的风险,从而导致固定失效。因此,需保证缝线具有足够的强度。缝线强度可通过缝线的断裂强力指标进行量化,其测试方法可参考YY/T 1832-2022《运动医学植入器械 缝线拉伸试验方法》。
(4)系统固定强度:根据不良事件汇总结果,系统固定失效的表现形式多样,包括固定锚(棒)从半月板中脱出、固定锚(棒)断裂、缝线断裂、滑结失效、缝线与固定锚(棒)分离等等,上述失效均可导致半月板缝合手术失败。因此,系统固定强度主要考虑全内半月板缝合系统在手术即刻及愈合过程中的足够稳定性。系统固定强度可通过疲劳前后固定强度、疲劳后缝合处的位移量进行量化。建议模拟临床使用及产品预期作用期限制定相应的试验加载载荷和循环周期等参数,部分文献也给出了一些试验方法(如试验模型、加载载荷、频率和加载周期)可供参考。考虑到体外测试受到诸多试验条件的限制,如半月板模型的选择、加载模型及加载方式、测试环境等,体外测试无法完全模拟体内的情况。针对该性能进行体外测试主要是完成产品设计验证的工作。可以对比不同生产商相似设计的产品的性能,力学测试结果的可接受性建议优先选择结构、尺寸及材料相近的同类已上市产品进行对比,此外也可以接受有学术共识或文献支持性依据的结果。无论选择哪种方法,需注意试验方法的一致性,如半月板模型选取、加载载荷和加载周期,确保试验结果具有可比性。
2.生物相容性
全内半月板缝合系统包括植入类组件(如固定锚(棒)和缝线)和与人体短暂接触类组件(如配套工具等)。预期与人体接触的部分,需要根据接触类型开展生物学评价,必要时进行生物学试验,建议根据GB/T 16886.1-2022《医疗器械生物学评价 第1部分: 风险管理过程中的评价与试验》系列标准对产品的生物相容性进行评价。可参考《医疗器械生物学评价和审查指南》(国食药监械[2007]345号)的相关要求阐明实施或豁免生物学试验的理由。
该部分内容需要注意的是,在既往的注册申报过程中,经常也会遇到采用原材料的生物学试验报告完成申报产品的生物学评价的情形,如采用纱线的生物学试验报告完成缝线的生物学评价,需要论证从纱线编织成缝线的生产工艺过程及后续包装灭菌过程不会引入新的生物学风险。
3.动物试验
动物试验是评价医疗器械安全有效的重要手段之一,针对全内半月板缝合系统是否开展动物试验建议参考《医疗器械动物试验研究技术审查指导原则第一部分:决策原则》。对于多数的不可吸收全内半月板缝合系统,如果通过理化表征、性能验证等手段证明其技术特性与市售同类产品具有等同性,通常不需要进行动物试验。
4.灭菌确认和稳定性
全内半月板缝合系统一般以无菌状态交付,灭菌方式通常采用辐照灭菌或环氧乙烷灭菌。申请人需提供灭菌确认资料,具体要求可参考GB 18279、GB 18280系列标准。此外,无菌状态交付的产品需按照《无源植入性医疗器械稳定性研究指导原则》提供稳定性研究资料,可采用实时老化或加速老化的方法。需要注意的是,对于多组件的产品可能存在不同包装的情形,这种情况下应针对每种包装分别提交资料。
(三)临床评价
全内半月板缝合系统需按照《医疗器械临床评价技术指导原则》及《免于进行临床评价的医疗器械目录》来选择合适的临床评价路径。对于多数的全内半月板缝合系统而言,可免于进行临床评价。但如果通过非临床研究无法证明产品的临床安全有效性或者在动物试验中发现仍需要提供临床证据的情况下,有可能需要通过开展申报产品的临床试验以完成临床评价。
如有第三类医疗器械注册咨询服务需求,欢迎您随时方便与杭州证标客医药技术咨询有限公司联络,联系人:叶工,电话:18058734169,微信同。