医疗器械标签标识尽管简单,但因为及其重要,也最直观,也是最容易被监管到的错误事项,因此,了解并正常使用符合MDR法规的标签标识,对医疗器械CE认证?企业来说非常重要。
医疗器械标签标识尽管简单,但因为及其重要,也最直观,也是最容易被监管到的错误事项,因此,了解并正常使用符合MDR法规的标签标识,对医疗器械CE认证企业来说非常重要。
与 MDD指令( 93/42/EEC )相比, MDR的标签需要更多信息,因为设备安全性和临床有效性数据需要与用户(医务人员和患者/最终用户)透明共享)。欧盟 MDR附件 I 第 III 章“一般安全和性能要求”中涵盖了有关随医疗器械提供的信息的所有要求。根据欧盟医疗器械法规 (MDR)(第 2 条)中的定义,“标签”是指出现在器械本身、每个单元的包装上或产品包装上的任何书面、印刷或图形信息。多个设备。贴标签过程的目的是识别医疗器械及其制造商,并传达有关安全、使用和性能的基本信息。它适用于医疗设备的用户,包括专业人士和消费者,以及相关第三方。

医疗器械CE认证标签,一是确保涵盖所有必要的符号和信息。另一个是标签的大小。由于需要更多的符号和数据,最大的挑战将是如何将它们全部放在标签上。在标签设计过程中,请记住以下几点:标签和说明的媒介、格式、内容、易读性和位置必须与预期用户的技术知识、经验、教育或培训相匹配。此外,使用说明必须以预期用户易于理解的术语编写,并在适当的情况下补充附图和图表。标签可以以人类可读的格式提供,并且可以用机器可读的信息来补充。
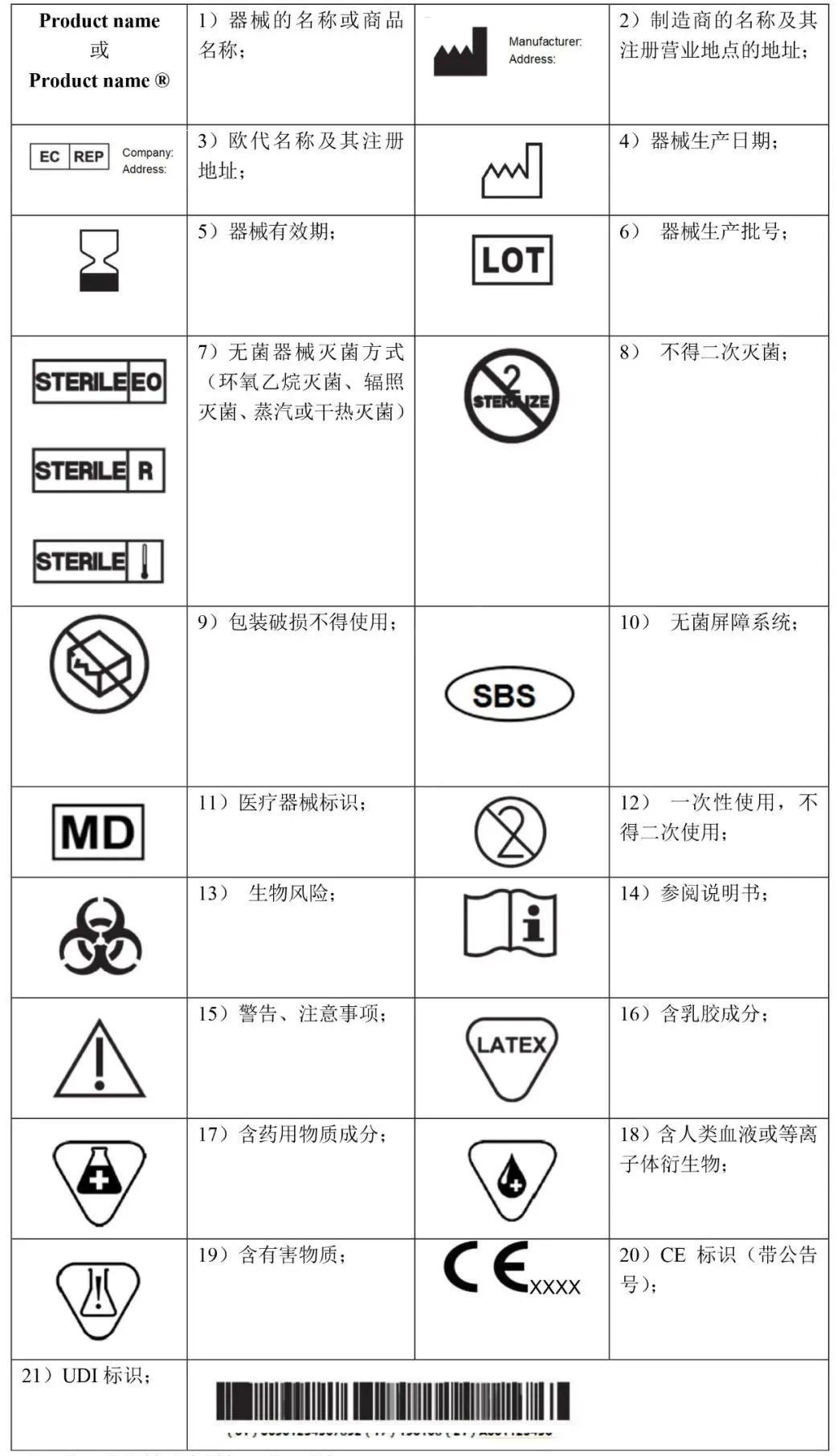
如下是常见标识。
任何有关医疗器械CE认证的需求,欢迎您随时方便与杭州证标客医药技术咨询有限公司联络!