医疗器械临床试验数据递交要求注册审查指导原则
一、前言
医疗器械临床试验数据是评价医疗器械安全有效性的重要支持性资料之一。规范地收集、整理、分析和递交医疗器械临床试验数据有助于提高临床试验实施和管理质量,同时有利于监管机构快速、高效地掌握临床试验的开展情况,提高审评效率。
为指导注册申请人规范递交临床试验数据及相关资料,以便更好地开展临床评价资料审评相关工作,制定本指导原则。
本指导原则是在现行法规和标准体系以及当前认知水平下制定的,随着法规和标准的不断完善,以及科学技术的不断发展,本指导原则的相关内容也将进行相应的调整。
二、适用范围
本指导原则适用于以产品注册为目的开展的医疗器械临床试验,包括在境外开展的医疗器械临床试验,不适用于按医疗器械管理的体外诊断试剂临床试验。与体外诊断试剂配合使用开展临床试验的体外诊断设备和软件,如将该临床试验用于该体外诊断设备和软件的注册申报,可参考本指导原则提交临床试验数据,亦可按照《体外诊断试剂临床试验数据递交要求注册审查指导原则》提交临床试验数据。本指导原则仅涉及临床试验数据递交相关内容,不涉及临床试验过程中数据管理相关要求。
三、基本原则
(一)真实原则
所递交的临床试验数据与临床试验原始记录保持一致。
(二)可追溯原则
按照注册申请人提交的数据、说明性文件和程序代码,可从原始数据库重现形成分析数据库、临床试验报告中的统计分析结果,且形成的分析数据库和统计分析结果与注册申请人提交的内容一致。
(三)可读原则
所提交数据库结构清晰,注释详尽,便于审阅。按照本指导原则相关规范要求递交临床试验数据有助于提高可读性。
四、临床试验数据相关资料及其说明
医疗器械临床试验数据相关资料通常包括原始数据库、分析数据库、说明性文件和程序代码,以下对各申报资料具体格式和内容提出要求。鼓励注册申请人参照临床数据交换标准协会(Clinical Data Interchange Standards Consortium, CDISC)标准递交数据。
外文资料提供中文翻译件时,对于原始和分析数据集,应至少翻译数据集、变量标签、观测值中的描述性文本(如不良事件描述等)。
(一)原始数据库
递交的原始数据库通常包含从病例报告表和外部文件中直接收集的原始数据,缺失的数据在此处不应进行填补。
原始数据库通常由多个不同的原始数据集组成,单个原始数据集是相同主题下多个变量的集合,这些变量的观测值共同形成该原始数据集,例如,人口学资料数据集可包括年龄、性别、身体质量指数(Body Mass Index,BMI)等。不同临床试验涉及的原始数据库不完全相同。单个原始数据集应收集相同主题下的变量,不同主题变量建议分别形成原始数据集,例如,膝关节Lysholm评分和IKDC2000评分相关变量建议分别形成两个原始数据集。
各数据集需包括受试者唯一标识变量,以实现同一受试者不同数据集观测值的关联。如涉及不同访视时间点观测的数据,应使用访视时间变量进行标识。例如,术后3个月和6个月心脏超声相关观测值,访视时间标识变量可命名为Visit_3、Visit_6等进行区分。若涉及两个及两个以上临床试验,数据集中需包括临床研究标识变量。若临床试验采用了随机分组,原始数据库中应包含随机号等变量。
数据集和变量命名应遵循“可读性”的原则,建议在对其命名时参考数据集或变量的英文或拼音,使得通过名称可较容易联想到该命名的实际含义。例如,可参考“Medical History”将病史数据集命名为“MH”,参考“Concomitant Medication”将合并用药数据集命名为“CM”,将变量“性别”命名为“sex”,变量“受试者姓名缩写”命名为“sub_abbr”等。
(二)分析数据库
分析数据库是为便于统计分析使用原始数据集形成的数据库,用于产生临床试验报告中的统计结果(包括基线、疗效和安全性指标统计分析等)。分析数据库主要包括原始数据库中的变量数据和按照临床试验方案和统计分析计划(如有)中事先确定的方法(如缺失值填补、量表子项评分加和等)从原始数据库变量数据衍生的数据。
分析数据库通常由多个不同的数据集组成,这些数据集一般与临床试验报告中的统计结果相对应。例如,临床试验报告中美国国立卫生研究院卒中量表(NIHSS)评分统计结果可对应专门的分析数据集,该分析数据集是为了生成NIHSS评分统计结果而专门创建的,包含生成该统计结果的全部变量数据,其他不相关变量数据不纳入到该数据集中。为了便于统计分析复验,分析数据集中的变量应具有可溯性,变量结构应清晰,不需繁琐的数据前处理即可开展统计分析。
分析数据集可基于其产生的相应统计结果进行命名,例如,生成不良事件比较结果的数据集可命名为“ADAE”(不良事件分析数据集)。建议在分析数据集名称中加入“AD”(analysis data)前缀,以标识该数据集为分析数据集。
分析数据集变量命名同原始数据库要求。注意明确不同分析集(如全分析集FAS、符合方案集PPS和安全分析集SS等)标识变量,以及形成数据库过程中产生的系统变量(如有),如序号、时间等。
(三)程序代码
需递交的代码主要包括:用于原始数据库生成分析数据库的代码、分析数据库生成统计分析结果的代码等,用于调整格式或生成表格的相关代码可不递交。递交的代码应符合通常的编程格式和编程规范,结构清晰明了,易于阅读。程序代码中应包括充分的注释,以描述不同程序代码的目的及其他需解释的内容,帮助审阅者更好地理解代码逻辑。如果递交的程序代码引用了宏程序,需提供相应的宏程序代码,并说明运行该程序的软件版本、系统环境。
(四)说明性文件
1.数据说明文件
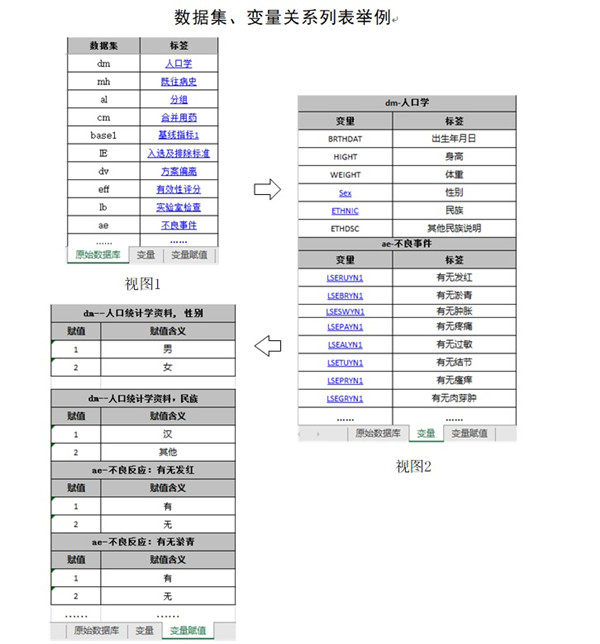
数据说明文件用于描述原始数据库和分析数据库的内容和结构,有助于审阅者快速了解数据库中各数据集、变量及其相互间的结构关系,准确理解递交的数据内容。建议采用Excel文件,以表格的形式分别列明原始数据库和分析数据库中所含的数据集、变量、变量类型(如字符型、数值型)、标签、赋值及其对应关系,具体可参考附录1《数据集、变量关系列表举例》。为了便于审阅,数据集和变量应具有相应的中文标签,标签长度不宜过长。若使用了外部词典(如MedDRA),应明确使用的外部词典名称和版本号。
分析数据库的说明文件需列明衍生变量的生成规则,明确涉及到的变量和计算方法。例如,对缺失值的填补,应明确填补方法,提供相应的程序代码。建议以表格的形式列明生成各分析数据集所用到的程序代码文件和原始数据集名称。
2.程序代码使用说明文件
程序代码使用说明文件用来解释说明程序代码文件使用方法、系统及软件环境,包括使用代码文件时是否需修改以及如何修改程序代码。同时,以表格形式逐一列明生成各统计结果图表所使用到的程序代码文件和数据集文件名称。
注册申请人应说明原始数据集和分析数据集所用编码(如UTF-8、EUC-CN等),以避免所递交的数据集出现乱码的情形。
3.注释病例报告表
相对于空白CRF,注释CRF增加了注释内容,反映了数据库中变量与CRF信息收集的对应关系。例如,在性别空白处注释变量名称sex。利用注释CRF,审阅者可直观地查阅各变量在CRF中的位置。CRF中可能收集了一些与临床试验结果分析无关的冗余数据,这些数据可不包含在递交的数据库中,但应在注释CRF上明确标注为“不递交”,并阐明理由。
4.其他说明性文件
除以上说明性文件外,鼓励注册申请人提交其他有利于审阅者快速了解临床试验数据库内容和结构的说明性文件(如概览性文件、其他特殊情况说明文件等)。
五、递交形式
原始数据库、分析数据库、说明性文件和程序代码分别放置于四个文件夹中。
原始数据库和分析数据库建议采用XPT[1]数据传输格式递交,建议全部原始数据集形成一个XPT文件,全部分析数据集形成一个XPT文件。建议采用XPT第5版本(简称XPT V5)或以上版本作为数据递交格式。
数据说明文件可采用PDF、Word、Excel等文件格式,其中变量词典建议采用Excel文件,注释病例报告表建议采用PDF文件。
程序代码建议采用TXT文件格式。
六、起草单位
国家药品监督管理局医疗器械技术审评中心。