欧盟一类医疗器械CE认证需要技术文件吗
发布日期:2021-05-25 23:20浏览次数:3402次
明天是2021年5月26日,是欧盟医疗器械法规MDR EU 2017/745因新冠疫情推迟一年后正式实施的日期。对于一类医疗器械,很多客户类比成国内备案,认为非常简单。从专业角度来看,一类医疗器械CE认证?与国内备案有先沟通之处,但也存在较大差异。
引言:明天是2021年5月26日,是欧盟医疗器械法规MDR EU 2017/745因新冠疫情推迟一年后正式实施的日期。对于一类医疗器械,很多客户类比成国内备案,认为非常简单。从专业角度来看,一类医疗器械CE认证与国内备案有先沟通之处,但也存在较大差异。
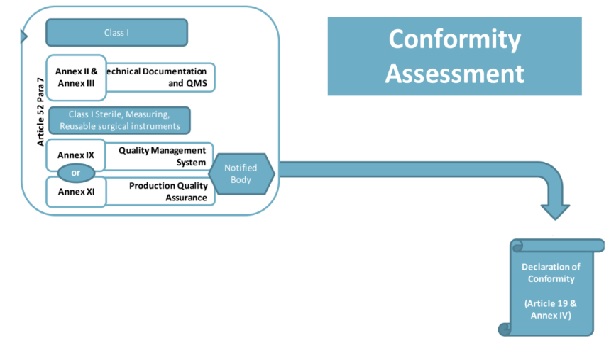
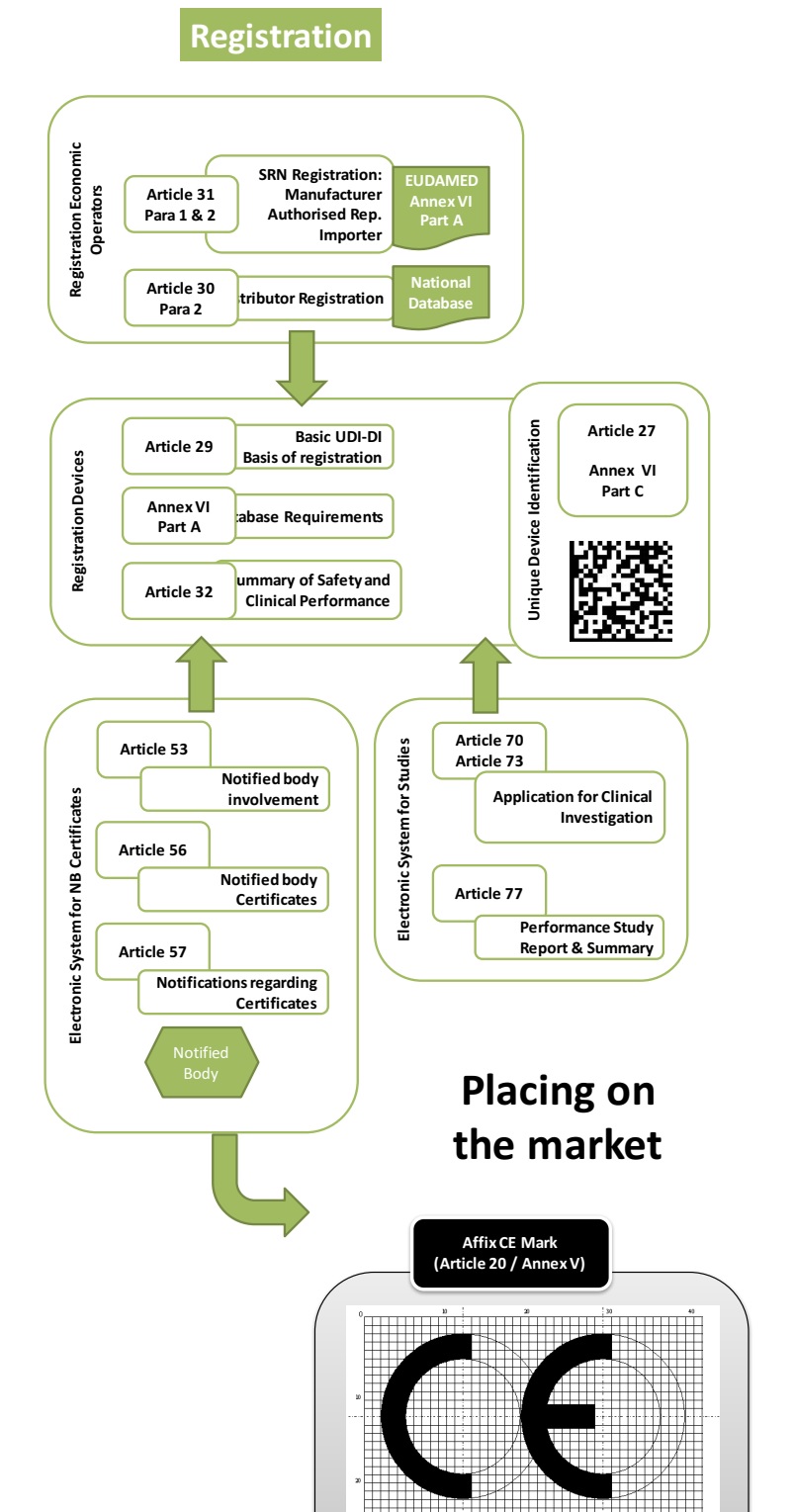
按照MDR的规定,对于自我宣告类器械,需要指定欧盟授权代表并完成器械注册后,才可以合法加贴CE标志并上市销售。下图是欧盟医疗器械注册流程图: