医疗器械临床试验、体外诊断试剂临床试验法规及监管制度来源于药品临床试验法规,但是由于产品的特性及风险差异较大,医疗器械临床试验法规与药品、体外诊断试剂临床试验法规又存在较大差异,我们一起来看一下。
引言:医疗器械临床试验、体外诊断试剂临床试验法规及监管制度来源于药品临床试验法规,但是由于产品的特性及风险差异较大,医疗器械临床试验法规与药品、体外诊断试剂临床试验法规又存在较大差异,我们一起来看一下。
一、药品、体外诊断试剂、医疗器械临床试验法规见下图:
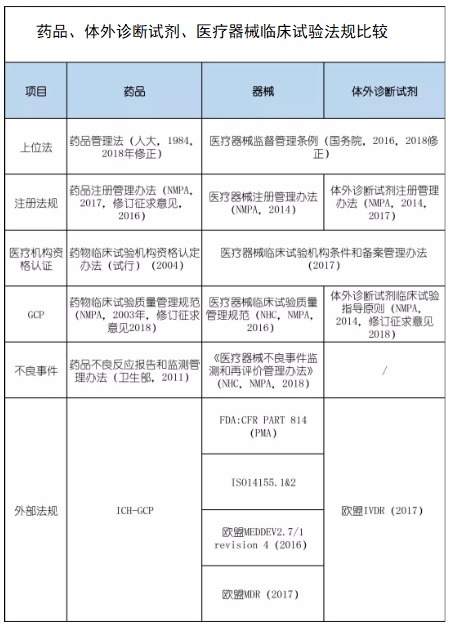
二、医疗器械临床试验法规与药品、体外诊断试剂法规的差异说明:
1、首先,我们看到,医疗器械临床试验法规与体外诊断试剂在国内基本一致,在国外则存在差异。
2、医疗器械临床试验质量管理规范及体外诊断试剂临床试验指导原则来源于药物临床试验管理规范,但与其又存在较大差异,特别是在临床试验分期方面。
3、不良事件层面,主要是报告对象及事故处理方面存在较大差异。
4、注册法规层面,药品与医疗器械、体外诊断试剂存在较大差异,医疗器械与体外诊断试剂基本一致。