浙江省第二类医疗器械注册变更资料要求
发布日期:2021-12-27 16:16浏览次数:3123次
医疗器械注册变更分为第二类医疗器械注册登记事项变更和第二类医疗器械注册登记事项变更,不同类型的变更无论是变更流程还是要求差异非常大,本文为大家介绍浙江省有关许可事项的第二类医疗器械注册变更资料要求。
医疗器械注册变更分为第二类医疗器械注册登记事项变更和第二类医疗器械注册登记事项变更,不同类型的变更无论是变更流程还是要求差异非常大,本文为大家介绍浙江省有关许可事项的第二类医疗器械注册变更资料要求。
一、第二类医疗器械注册许可变更事项的归口管理机构及相关事项(如下图所示):
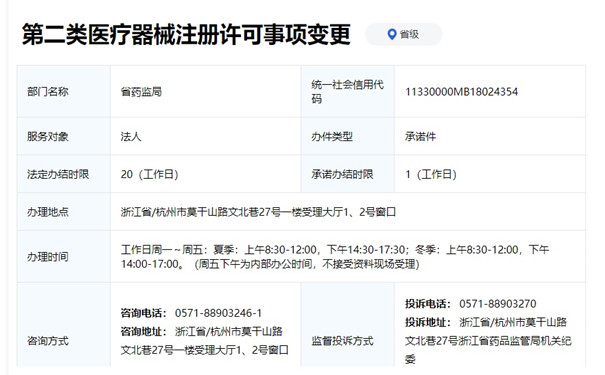
二、浙江省第二类医疗器械注册变更资料要求:
1.浙江省第二类医疗器械注册变更申请表;
2.注册人关于变更情况的声明;
3.原医疗器械注册证及其附件、历次医疗器械注册变更文件。
4.变更申请项目申报资料。
5.与产品变化相关的安全风险管理报告。
6.变化部分对产品安全性、有效性影响的资料。
7.针对产品技术要求变化部分的注册检验报告。
8.具体变更情况的其他技术资料要求。
9.符合性声明。